编者荐语:
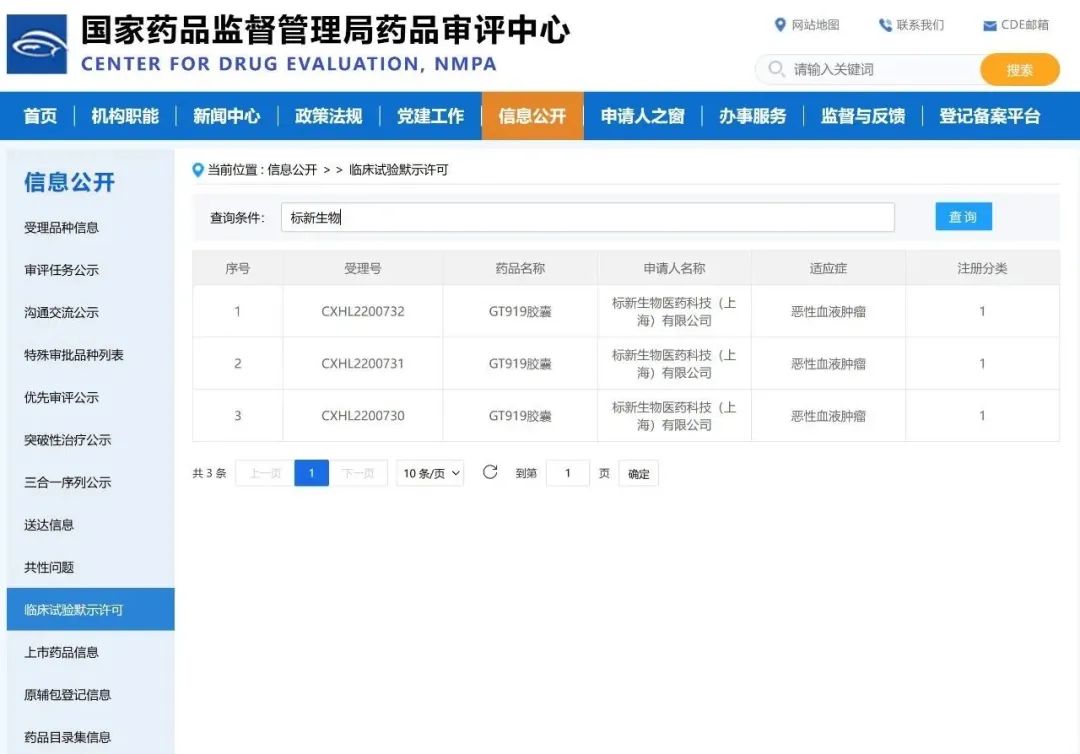
2022年12月20日,上科大孵化企业标新生物首个具有口服特性的蛋白降解管线GT919获得CDE的临床试验默示许可。2020年,标新生物医药科技(上海)有限公司成立并连续获得风险投资逾亿元,与上科大签订了超亿元合同金额的专利独家许可协议,此次是上科大成果转化项目获得的首个中国临床批件。
以下文章来源于标新生物GLUETACS

编者荐语:
2022年12月20日,上科大孵化企业标新生物首个具有口服特性的蛋白降解管线GT919获得CDE的临床试验默示许可。2020年,标新生物医药科技(上海)有限公司成立并连续获得风险投资逾亿元,与上科大签订了超亿元合同金额的专利独家许可协议,此次是上科大成果转化项目获得的首个中国临床批件。
以下文章来源于标新生物GLUETACS

